|
Güneş ışınları yer
yüzüne ulaşınca, üzerine düştüğü taş, toprak, su gibi maddeler ısınır;
ışınların bir kısmı ısıya dönüşür. Yazın çok ısınan taş, kum, toprak gibi
maddelerin sıcaklığı artığından üzerine çıplak ayakla basamayız. Isıtılan
bakır tencerenin de bir süre sonra sıcaklığı artarak, elimizi yakacak duruma
gelir. Yeteri kadar ısıtılmış olan odun ya da kağıt parçası ise tutuşur.
Petrol ürünleri,
odun, kömür gibi yakıtların yapılarındaki enerji, bu yakıtlar yandığında
ısıya dönüşür.
Elektrik enerjisi, maddenin
iç enerjisi, ışık enerjisi, ses enerjisi, güneş enerjisi gibi ısı da bir
enerji çeşididir. Yemek pişirmede, ısınmada, makinelerin, motorların,
fabrikaların,santrallerin çalıştırılmasında bu ısıdan yararlanırız. Isı
enerjisini üretebilmek için önce diğer bir enerji türünün tüketilmesi
gerekir. Söz gelişi kömür yanmadan ısı enerjisi elde edemeyiz. Yanma
sırasında kömürdeki kimyasal enerji ısı enerjisine dönüşür.
Elektrik enerjisi;
elektrik ocağı, ütü, ısıtıcı, fırın gibi araçlardaki tellerde ısıya dönüşür.
Biz de bu enerjiyi çeşitli işlerimizi yapmada kullanırız.
Maddeler katı, sıvı
ve gaz olmak üzere üç halde bulunurlar. Her üç halde de maddelerin
moleküllerinden ve atomlardan oluştuğunu biliyoruz.
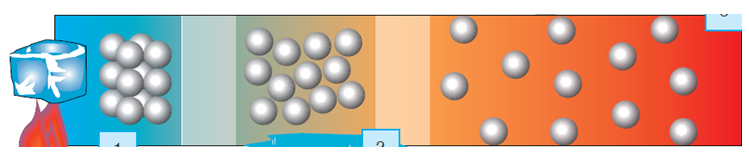
Katı bir maddenin
molekülleri bulundukları yerde titreşim hareketi yapar. Sıvının molekülleri
birbiri üzerinde kayarak yer değiştirirler. Gazlarda ise moleküller
bulundukları kabın içinde bağımsız olarak her yöne hareket ederler. İster
katı, ister sıvı, ister gaz halinde olsun, belli sıcaklıktaki her maddenin
molekül ve atomları hareketlidir.
Molekül ya da
atomlar değişik hızlarla hareket ettiklerinden hepsinin hızları birbirine
eşit değildir. Buna göre her atom ya da molekülün ortalama bir kinetik
enerjiye sahip olduğunu söyleyebiliriz.
Her bir molekülün
sahip olduğu kinetik enerjinin değeri çok küçüktür. Bu nedenle tek tek
moleküllerin kinetik enerjilerini hissedemeyiz. Herhangi bir maddeyi
oluşturan moleküllerin sayısı oldukça fazladır. Sayılamayacak kadar çok
sayıdaki moleküllerin kinetik enerjilerinin toplamı çok büyük değerlere
ulaşır. Biz bu toplam enerjiyi ölçebiliriz.
Büyün moleküllerin
sahip olduğu kinetik enerjilerin toplamını o maddeyi oluşturan molekül
sayısına böleriz. Böylece molekül başına düşen ortalama kinetik enerjiyi elde
ederiz. Bu da bize o maddenin sıcaklığı hakkında bir fikir verir.
Moleküllerin
hareketleri arttıkça, kinetik enerjileri artar. Bu ise molekül başına düşen
ortalama kinetik enerjinin; kısaca sıcaklığın artmasıdır. Buna göre sıcaklık
bir maddedeki moleküllerin ortalama kinetik enerjileri ile ilgili bir
büyüklüktür.
Bir maddeye ısı
verildiğinde moleküllerin hareketi hızlanır ve kinetik enerjileri artar.
Kısaca moleküller kinetik enerji kazanır. Böylece ısı enerjisi kazanan
maddelerin sıcaklıkları yükselir.
Soğuyan maddelerde
ise moleküllerin hareketi yavaşlar. Bu da moleküllerin kinetik enerjilerinin
azalması demektir. Isı enerjisi kaybeden maddelerin sıcaklıkları düşer.
Anlatılanlardan
da anlaşılacağı gibi ısı ile sıcaklık aynı kavramlar değildir. Buna örnek
verelim.
Kaynamakta
olan çaydanlıktaki sudan bir çay bardağı su alalım. Çaydanlıktaki ve çay
bardağındaki suların sıcaklıkları aynıdır. Fakat ikisindeki ısı miktarları
birbirine eşit değildir. Çaydanlıktaki sıcak su ile daha çok buz
eritebiliriz. Bir bardak sıcak su ile eritilen buz çok azdır. Çaydanlıktaki
suyun ısısı bir bardak suyun ısısından daha fazladır.
SICAKLIK
Bir cismin ne kadar
sıcak olduğunun ölçüsüdür. Derideki duyu alıcılarının yardımıyla bir cismin
sıcaklığı konusunda kabaca da olsa bir izlenim denebilir. Ama sıcaklığın tam
olarak bilinmesinin gerektiği işlerde ya da derinin dayanabileceğinden daha
sıcak ve daha soğuk cisimlerin ölçümünde termometre kullanılır. Sanayi
fırınlarındaki gibi çok yüksek sıcaklıkların ölçümünde ise pirometrelerden yaralanılır.
Termometrenin
üzerinde bir sıcaklık ölçeği vardır. Pek çok ülkede kullanılan Celsius
ölçeğine göre, buzun erime noktası 0 derece, suyun kaynama noktası 100
derecedir. Bugün ABD`de kullanılmakta olan Fahrenheit ölçeğine göre buzun
erime noktası 32 derece, suyun kaynama noktası ise 212 derecedir. Kelvin ise
bilim adamlarının kullanır.
Bir cismin
sıcaklığı moleküllerinin titreşim hızına bağlıdır. Molekülleri ne kadar hızlı
titreşirse cisim o kadar sıcak, ne kadar yavaş titreşirse cisim o kadar soğuk
olur. Moleküller hareket halinde olduklarından kinetik enerjiyi sahiptir. Bir
cismin sıcaklığı moleküllerinin ortalama enerjisini gösterir. Eğer herhangi
bir cisim, moleküllerinin tamamen hareketsiz hale geleceği ve tüm hareket
enerjilerini yitireceği bir noktaya kadar soğutulabilseydi, böyle bir noktada
artık hiçbir iç enerji bulunmazdı. Hiçbir cisim bundan daha soğuk olamaz.
Mutlak sıfır denen bu sıcaklık yaklaşık –273 santigrat derecedir. Mutlak
sıfıra ulaşmak imkansızdır; ama bilim adamları bu noktanın derecenin milyonda
biri kadar yakınına ulaşabilmeyi başarabilmişlerdir.
Diğer bütün
memeliler ve kuşlarda olduğu gibi, insan vücudu da çevre sıcaklığından
bağımsız olarak belli bir sıcaklığı korur ve bu sıcaklık pek az değişir.
İnsanın normal vücut sıcaklığı 36,9 santigrat derecedir. Normal vücut
sıcaklığı insandan insana ve ölçümün yapıldığı vücut bölgesine göre çok hafif
bir değişim gösterir.
Sıcaklığın
Ölçülmesi
Kaynamakta olan
çaydanlığa elinizi dokunmaktan sakınırız. Çünkü onun çok sıcak olduğunu ve
elimizi yakacağını biliriz. Bir buz parçasını elimize aldığımızda elimizin
üşüdüğünü hisseder, buzun çok soğuk olduğunu belirtiriz.
Buna göre bir
maddenin sıcak ya da soğuk olması, onun sıcaklık derecesi ile ilgilidir.
Sıcak olan bir maddenin sıcaklık derecesi yüksek, soğuk olanın ise sıcaklık
derecesi düşüktür.
İki maddeden
hangisinin sıcak ya da soğuk olduğunu dokunma duyumuzla anlayabiliriz. Fakat
her sıcaklığı ölçmede dokunma duyumuz yeterli olmayabilir. Dokunma duyumuzun
dayanabileceği sıcaklık derecesine kadar olan sıcaklıklar ile ilgili kabaca
bir fikir ediniriz. Bunu da sıcak, soğuk, ılık biçiminde belirtiriz. Dokunma
duyumuzu kullanarak sayısal bir değer vererek yanılma ihtimali yüksektir.
Bu nedenle sıcaklık
ölçülürken, kesin ve doğru değerler veren araçlar kullanılır. Bir maddenin
sıcaklık derecesini sayıyla gösterebilen bu araçlara termometre adı verilir.
Termometre
Çeşitleri
Isınınca
genleşmeleri sıcaklıkla orantılı olan katı, sıvı, gaz maddelerden çeşitli
termometreler yapılmıştır. Çok yaygın olarak kullanılan sıvılı ve metal
termometrelerdir.
Sıvılı
Termometreler:
Sıvılı
termometrelerde genleşmeleri büyüyen ve sıcaklıkla orantılı olan sıvılar
kullanılır. İnce cam boru içindeki sıvı; cıva ise cıvalı termometre, alkol
ise alkollü termometre adını alır.
Cıva –39 santigrat
derecede donar, 357 santigrat derecede kaynar. Cıvalı termometreler ile –39
santigrat derece ile 357 santigrat derece arasındaki sıcaklıkları
ölçebiliriz. Çok soğuk kış günlerinde bu termometreler kullanılmaz. Bunu
yerine donma sıcaklığı daha düşük olan alkollü termometreler kullanılır.
Çünkü alkol yaklaşık olarak-115 santigrat derecede donar. Bu termometreleri
kutuplarda kullanmak mümkündür. Ancak kılcal boru içindeki sıvının iyi
görülebilmesi için kırmızı, mavi, sarı vb. renkli boya maddeleri ile
boyanması gerekir. Sıvılı termometreler kullanıldıkları yerlere göre çeşitli
isimler alırlar. Duvar termometresi, laboratuar termometresi ve hasta
termometresi gibi.
Hasta
Termometresi:
Cıvalı bir
termometredir. Vücut sıcaklığını ölçmede kullanılır. 35 santigrat derece ile
42 santigrat derece arasındaki sıcaklıkları 1/10 incelikle ölçer. Bu
termometrelerin haznesi ile kılcal borunu birleştiği yerde bir boğum bulunur.
Vücut sıcaklığı ölçüldükten sonra termometre sapından tutularak sallanır.
Neden? Yeni bir ölçmeye hazır olan termometre ağız içi ya da koltuk
altına konularak vücut sıcaklığı ölçülür.
Metal
Termometre:
Cıvalı ve alkollü
termometreler ile ölçülemeyen sıcaklık derecelerini ölçmek için metal
termometreler kullanılır. Metal termometreler ile 1600 santigrat dereceye
kadar olan yüksek sıcaklıklar ölçülebilir. Fabrika ve fırınlar kullanıldığı
yerlerdir.
GÜNLÜK
HAYATIMIZDA ISI VE SICAKLIK
Bir kibrit alevi
ile yemeğimizi pişiremeyiz. Genellikle evlerimizdeki ocaklarda 12 kg’lik
tüpler içinde sıvılaştırılmış petrol gazı kullanırız. Bu tüp içindeki gaz
yandığında yaklaşık 40 gün yemeğimizi pişirebiliriz. Aynı gazı verdiği ısı
ile odamız 7-8 gün ısıtılabilir. Çünkü tüpün içindeki ısı kibrit alevinin
verdiği ısıdan çok fazladır. Bir ton taş kömürünün verdiği ısı, iki ton
linyitin verdiği ısıdan daha fazladır. Bu yüzden ton başına fiyatı
linyitin iki katı da olsa linyit yerine taş kömürü alan karlıdır. Çünkü aynı
para ile daha çok ısı satın almaktadır. Sonuç olarak ısı alınıp satılan bir
enerji çeşidi olmaktadır. Isı enerjisi doğrudan ölçülemez. Isı miktarı
hesapla bulunur. Birimi joule ‘dir. Isıyı ölçmede kullanılan araç ise
kalorimetredir.
Her gün
dinlediğimiz hava raporlarında derece santigrat cinsinden verilen değerler
sıcaklıklardır. Giyimimizi havanın sıcaklığına göre ayarlarız. Denize
girerken bizim için önemli olan suyun sıcaklığıdır. Sıcak maddenin, soğuk
maddeden daha yüksek olan özelliği sıcaklığıdır. Maddelerin sıcaklığı
doğrudan ölçülebilir. Sıcaklığı ölçmede kullanılan araç termometredir. Birimi
ise santigrat derecedir.
Bir
Cismin Sıcaklığının Artmasını Sağlayan Fiziksel
Enerji: ISI
Isı bir cismin
sıcaklık derecesini belirten enerjidir. Isı miktarıyla sıcaklık doğru
orantılıdır. Bir cismin üzerindeki ısı arttıkça o cismin sıcaklığı da artar.
Fizik biliminin
büyük dallarından biri de ısı bölümüdür. Dünyamızda geçen hemen hemen her
olayda ısı önemli bir yer tutar, insanların yer yüzünde ilk olarak
karşılaştıkları tabiat olaylarından biri de ısı olmuştur.
İnsanlar, tabiat
olaylarının sebeplerini, kanunlarını araştırmaya başladıktan sonra, ısının ne
olduğunu da merak ettiler. Önceleri ısıyı bir cisim sandılar. Ancak deneyler
ısının ağırlığının olmadığını gösteriyordu. Isıtmadan önce, ısıttıktan sonra
tarttıkları cisimlerin ağırlığında bir değişiklik görmediler. Öyleyse ısı
gözle görülmeyen, ağırlığı olmayan, sıcak bir cisimden soğuk bir cisme
geçebilen yani akışkan bir cisimdir. Buna kalorik adını verirler. 1800 yılına
kadar bu inanış sürüp geldi. Ancak, bundan sonra ısının cisim olmadığını
gösteren deneyler yapıldı.
Isı
Üzerinde Deneyler:
Bu deneylerden
ilkini aslında Amerikalı olan, bağımsızlık savaşında İngilizleri tuttuğu için
sonradan İngiltere’ye kaçan Kont Rumford yaptı. Eskiden topları silindir
biçimindeki demirlerin ortasını oyarak yaparlardı. Bu delme işlemi sırasında
yem demir sinindir hem de deliği açan torna kalemi ısınır. Bu olaya dikkat
eden Rumford ısı cisminin nereden geldiğini araştırdı. Topun çevresine ısı
geçirmeyen keçe sardı, gene ısı meydana geliyordu. Kalemin hızını arttırdı,
sıcaklık daha yükseldi. Bu gözlem sonunda Rumford şu sonuca vardı: dışarıya
karşı yalıtılmış bir cisim kendi kendine bir cisim doğuramaz: öyleyse ısı bir
cisim değil harekettir.
Bundan sonra gene
İngiliz bilgini Sir Humphrey Davy çok soğuk bir kış gecesi, iki buz parçasını
birbirine sürtünce, buzların eridiğini gördü. Deneyi düşük sıcaklıkta bir
daha yaptı, buzlar gene eridi. Buz ancak 0 derecenin üstünde eridiğine göre
sürtme sonunda buzların sıcaklığı 0 derecenin üstüne çıkmıştı. Başka bir
cisimle bağlantısı bulunmayan buzlara ısı cismi nereden geliyordu? Bu sorunun
karşılığını arayan Davy de ısının bir cisim olmadığı sonucuna vardı. Daha sonra
İngiliz Juole’un da bir kap içindeki karıştırarak ısıtmasıyla ısının cisim
olmadığı artık iyice anlaşılmış oldu.
Isı
Nedir:
Bugün artık
herkesin kabul ettiği kurama göre ısı, bir çeşit enerjidir. Bilindiği bütün
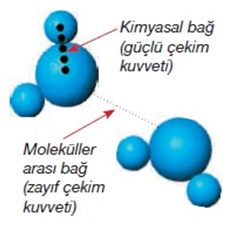
cisimler moleküllerden, onlarda atomlardan meydana gelirler. Bu moleküller de
değişmez değillerdir; sürekli olarak hareket halindedirler, kaynaşırlar. Bu
kaynaşmaları moleküllerde kinetik enerji bulunduğunu gösterir. Bazı
moleküllerde potansiyel enerji de vardır. Bir cisme dışardan ısı enerjisi verirsek,
cismin toplam kinetik ve potansiyel enerjisinde bir değişme olmaz. Bu enerji
moleküllere geçer, onların hareketini güçleştirir. Bu yüzden, birbirine
sürtülen iki cisim ısınır. Sürtünmeyle verilen enerji, moleküllerin
hareketini arttırır, bunu sonunda da cisimler ısınır. Çekiçle dövülen demirin
ısınması da bundandır. Vurma sırasında cisimlere verilen enerji onların
moleküllerinin artırmış, dolayısıyla cisimleri ısıtmıştır.
Demek ki ısı bir
enerjidir. Katı ve sıvı cisimlere verilirse onların moleküllerinin hem
kinetik, hem de potansiyel enerjiler4ini arttırır. Gaz halindeki cisimlere
verilirse moleküllerin yalnız kinetik enerjisi artar.
Isının
Cisimler Üzerindeki Etkileri
1 ) Katılarda:
Bir cisme ısı
verilirse o cismin sıcaklık derecesi yükselir. Bunun için cisimlerin sıcaklık
derecesi belirtilmiştir. Saf suyun donduğu sıcaklık derecesi 0, kaynadığı
sıcaklık derecesi de 100 kabul edilmiştir. Bu iki değerin arası 100 eş
parçaya bölünmüştür. Bu bize santigrat sıcaklık derecesini verir. C ile gösterilir.
Bundan başka Fahrenhayt ve Reomür sıcaklık dereceleri vardır.
Uzatma Katsayısı.
Genel olarak, cisimlere ısı verilince boyutları uzar. Bir maden çubuğu bütün
uzunluğu boyunca ısıtıldıktan sonra ölçersek boyunun soğuk durumuna göre
arttığını görürüz. Bu uzama her cisimde aynı değildir. Aynı ısı değerleri
için cisimlerin uzamaları farklıdır. Bunu belirtmek için uzama katsayısı
kullanılır. Bir cismin birim uzunluğunun 1 santigrat derece sıcaklık farkında
uzadığı miktara o cismin uzama katsayısı denir.
2 )
Sıvılarda:
Sıvılar da
genel olarak ısı aldıkları zaman hacimce genleşirler. Yalnız, sıvıların belli
bir hacimleri olmadığı için bir kap içinde bulundurulurlar. Isıyla hacim
değişmesini incelerken kabın genleşmesini de göz önünde bulundurmak
gereklidir. Yoksa, bulunan sonuçlar yanlış olur.
Ergime Isısı. Katı
bir cismin birim kütlesini sıcaklığını değiştirmeden ergitmek için verilmesi
gereken ısı miktarına o cismin ergime ısısı denir. Bu değer su için 80
kaloridir. Yani, 1 gram buz 0 santigrat derecesinde ergirken çevresinden 80
kalori alır, 1 gram buz donarken çevresine 80 kalori verir.
Basıncın Etkisi.
Bir sıvının donma noktası sıvı üzerine yapılan basınçla değişir. Donma
sırasında büzülen sıvılarda basınç arttıkça donma noktası daha büyük
değerlere kayar. Donma sırasında genişleyen sıvılarda ise durum tersleşir.
Onun için, ısı problemlerinde basıncın da göz önünde tutulması gereklidir.
Kolaylık için
normal şartlar tarif edilmiştir. 76 sm. hava basıncı ve 0 santigrat
derecesine normal şartlar denir.
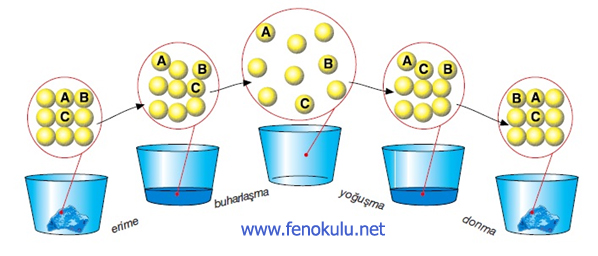
Buharlaşma Olayı.
Bir cismin gaz haline geçmesine buharlaşma olayı denir. Üç bölümü vardır;
1) Buharlaşma
2) Kaynama
3) Süblimleşme
1)
Buharlaşma: Sıvının
sadece yüzeyindeki kısımlarının buhar haline geçmesidir.
2)
Kaynama: Sıvının
yalnız yüzeyinde kalmayıp bütününe yayılan buharlaşmadır. Kaynama sonunda
bütün sıvı buhar haline geçer. Bir sıvıyı kaynatmak için ona ısı verilmesi
gerekir. Bir sıvının birim kütlesini sıcaklığı değişmeksizin, buhar haline
geçirmek için verilmesi gereken ısıya buharlaşma ısısı denir. Bu değer su
için 539 kaloridir; yani 1 gram suyu buharlaştırmak için ona 539 kalori
verilmelidir.
3)
Süblimleşme: belli
sıcaklık ve basınç altında bir cismin, katı halinden, doğrudan doğruya gaz
haline geçmesidir. Naftalin normal şartlarda bu özelliği gösterir.
|


 + 3.a.h
+ 3.a.h